2.3.Sifat-sifat koloid
3. Sifat-sifat Koloid
a. Efek Tyndall
Jika seberkas cahaya dilewatkan pada suatu sistem koloid, maka cahaya tersebut akan dihamburkannya sehingga berkas cahaya tersebut akan kelihatan. Sedangkan jika cahaya dilewatkan pada larutan sejati maka cahaya tersebut akan diteruskannya . Sifat koloid yang seperti inilah yang dikenal dengan efek tyndall dan sifat ini dapat digunakan untuk membedakan koloid dengan larutan sejati. Gejala ini pertama kali ditemukan oleh Michael Faradaykemudian diselidiki lebih lanjut oleh John Tyndall (1820 – 1893), seorang ahli Fisikabangsa Inggris.
Efek Tyndall juga dapat menjelaskan mengapa langit pada siang hari berwarna biru sedangkan pada saat matahari terbenam, langit di ufuk barat berwarna jingga atau merah. Hal itu disebabkan oleh penghamburan cahaya matahari oleh partikel koloid di angkasa dan tidak semua frekuensi dari sinar matahari dihamburkan dengan intensitas sama.
 Jika intensitas cahaya yang dihamburkan berbanding lurus dengan frekuensi, maka pada waktu siang hari ketika matahari melintas di atas kita frekuensi paling tinggi (warna biru) yang banyak dihamburkan, sehingga kita melihat langit berwarna biru. Sedangkan ketika matahari terbenam, hamburan frekuensi rendah (warna merah) lebih banyak dihamburkan, sehingga kita melihat langit berwarna jingga atau merah.
Jika intensitas cahaya yang dihamburkan berbanding lurus dengan frekuensi, maka pada waktu siang hari ketika matahari melintas di atas kita frekuensi paling tinggi (warna biru) yang banyak dihamburkan, sehingga kita melihat langit berwarna biru. Sedangkan ketika matahari terbenam, hamburan frekuensi rendah (warna merah) lebih banyak dihamburkan, sehingga kita melihat langit berwarna jingga atau merah.
Gejala efek tyndall yang dapat diamati dalam kehidupan sehari-hari adalah sebagai berikut:
– Sorot lampu mobil pada malam yang berkabut
– Sorot lampu proyektor dalam gedung bioskop yang berasap dan berdebu
– Berkas sinar matahari melalui celah pohon-pohon pada pagi yang berkabut
b. Gerak Brown
Gerak brown merupakan gerak patah-patah (zig-zag) partikel koloid yang terus menerus dan hanya dapat diamati dengan mikroskop ultra. Gerak brown terjadi sebagai akibat tumbukan yang tidak seimbang dari molekul-molekul medium terhadap partikel koloid.Dalam suspensi tidak terjadi gerak Brown karena ukuran partikel cukup besar, sehingga tumbukan yang dialaminya setimbang. Partikel zat terlarut juga mengalami gerak Brown, tetapi tidak dapat diamati. Semakin tinggi suhu, maka gerak brown yang terjadi juga semakin cepat, karena energi molekul medium meningkat sehingga menghasilkan tumbukan yang lebih kuat.
mikroskop ultra. Gerak brown terjadi sebagai akibat tumbukan yang tidak seimbang dari molekul-molekul medium terhadap partikel koloid.Dalam suspensi tidak terjadi gerak Brown karena ukuran partikel cukup besar, sehingga tumbukan yang dialaminya setimbang. Partikel zat terlarut juga mengalami gerak Brown, tetapi tidak dapat diamati. Semakin tinggi suhu, maka gerak brown yang terjadi juga semakin cepat, karena energi molekul medium meningkat sehingga menghasilkan tumbukan yang lebih kuat.
Gerak Brown merupakan faktor penyebab stabilnya partikel koloid dalam medium dispersinya. Gerak brown yang terus menerus dapat mengimbangi gaya gravitasi sehingga partikel koloid tidak mengalami sedimentasi (pengendapan).
c. Elektroforesis
 Partikel koloid dapat bergerak dalam medan listrik karena partikel koloid bermuatan listrik. Pergerakan partikel koloid dalam medan listrik ini disebut elektroforesis. Jika dua batang elektrode dimasukkan kedalam sistem koloid dan kemudian dihubungkan dengan sumber arus searah, maka partikel koloid akan bergerak kesalah satu elektrode tergantung pada jenis muatannya. Koloid bermuatan negatif akan bergerak ke anode (elektrode positif) sedang koloid bermuatan positif akan bergerak ke katode (elektrode negatif).
Partikel koloid dapat bergerak dalam medan listrik karena partikel koloid bermuatan listrik. Pergerakan partikel koloid dalam medan listrik ini disebut elektroforesis. Jika dua batang elektrode dimasukkan kedalam sistem koloid dan kemudian dihubungkan dengan sumber arus searah, maka partikel koloid akan bergerak kesalah satu elektrode tergantung pada jenis muatannya. Koloid bermuatan negatif akan bergerak ke anode (elektrode positif) sedang koloid bermuatan positif akan bergerak ke katode (elektrode negatif).
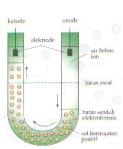 Elektroforesis dapat digunakan untuk mendeteksi muatan partikel koloid. Jika partikel koloid berkumpul dielektrode positif berarti koloid bermuatan negatif, jika partikel koloid berkumpul dielektrode negatif bearti koloid bermuatan positif. Peristiwa elektroforesis ini sering dimanfaatkan kepolisian dalam identifikasi/tes DNA pada jenazah korban pembunuhan/ jenazah tak dikenal
Elektroforesis dapat digunakan untuk mendeteksi muatan partikel koloid. Jika partikel koloid berkumpul dielektrode positif berarti koloid bermuatan negatif, jika partikel koloid berkumpul dielektrode negatif bearti koloid bermuatan positif. Peristiwa elektroforesis ini sering dimanfaatkan kepolisian dalam identifikasi/tes DNA pada jenazah korban pembunuhan/ jenazah tak dikenal
d. Adsorpsi
Adsorpsi adalah peristiwa di mana suatu zat menempel pada permukaan zat lain, seperti  ion H+ dan OH– dari medium pendispersi. Untuk berlangsungnya adsorpsi, minimum harus ada dua macam zat, yaitu zat yang tertarik disebut adsorbat, dan zat yang menarik disebut adsorban. Apabila terjadi penyerapan ion ada permukaan partikel koloid maka partikel koloid dapat bermuatan listrik yang muatannya ditentukan oleh muatan ion-ion yang mengelilinginya.
ion H+ dan OH– dari medium pendispersi. Untuk berlangsungnya adsorpsi, minimum harus ada dua macam zat, yaitu zat yang tertarik disebut adsorbat, dan zat yang menarik disebut adsorban. Apabila terjadi penyerapan ion ada permukaan partikel koloid maka partikel koloid dapat bermuatan listrik yang muatannya ditentukan oleh muatan ion-ion yang mengelilinginya.
 Partikel koloid mempunyai kemampuan menyerap ion atau muatan listrik pada permukaannya. Oleh karena itu partikel koloid bermuatan listrik. Penyerapan pada permukaan ini disebut dengan adsorpsi. Contohnya sol Fe(OH)3 dalam air mengadsorpsi ion positif sehingga bermuatan positif dan sol As2S3 mengadsorpsi ion negatif sehingga bermuatan negatif. Pemanfaatan sifat adsorpsi koloid dalam kehidupan antara lain dalam proses pemutihan gula tebu, dalam pembuatan norit (tablet yang terbuat dari karbon aktif) dan dalam proses penjernihan air dengan penambahan tawas.
Partikel koloid mempunyai kemampuan menyerap ion atau muatan listrik pada permukaannya. Oleh karena itu partikel koloid bermuatan listrik. Penyerapan pada permukaan ini disebut dengan adsorpsi. Contohnya sol Fe(OH)3 dalam air mengadsorpsi ion positif sehingga bermuatan positif dan sol As2S3 mengadsorpsi ion negatif sehingga bermuatan negatif. Pemanfaatan sifat adsorpsi koloid dalam kehidupan antara lain dalam proses pemutihan gula tebu, dalam pembuatan norit (tablet yang terbuat dari karbon aktif) dan dalam proses penjernihan air dengan penambahan tawas.
e. Koagulasi
Koagulasi adalah peristiwa pengendapan atau penggumpalan koloid. Koloid distabilkan oleh muatannya. Jika muatan koloid dilucuti atau dihilangkan, maka kestabilannya akan berkurang sehingga dapat menyebabkan koagulasi atau penggumpalan. Pelucutan muatan koloid dapat terjadi pada sel elektroforesis atau jika elektrolit ditambahakan ke dalam system koloid. Apabila arus listrik dialirkan cukup lama kedalam sel elektroforesis, maka partikel koloid akan digumpalkan ketika mencapai electrode. Koagulasi koloid karena penambahan elektrolit terjadi karena koloid bermuatan positif menarik ion negative dan koloid bermuatan negative menarik ion positif. Ion-ion tersebut akan membentuk selubung lapisan kedua. Jika selubung itu terlalu dekat, maka selubung itu akan menetralkan koloid sehingga terjadi koagulasi.
Beberapa contoh peristiwa koagulasi dalam kehidupan sehari-hari adalah:
– Pembentukan delta di muara sungai karena koloid tanah liat dalam air sungai mengalami koagulasi ketika bercampur dengan elektrolit dalam air laut.
– Karet dalam latek digumpalkan dengan menambahkan asam formiat
– Lumpur koloidal dalam air sungai dapat digumpalkan dengan menambahkan tawas
– Asap atau debu pabrik dapat digumpalkan dengan alat koagulasi listrik dari cottrel.




Leave a comment
Comments 0